РЕГЕНЕРАТИВНАЯ МЕДИЦИНА
КЛЕТОЧНАЯ ТЕРАПИЯ
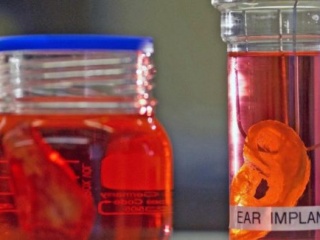
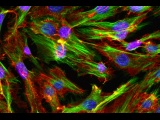
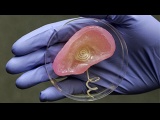
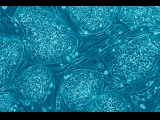
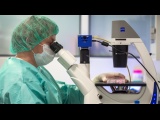
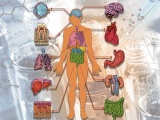
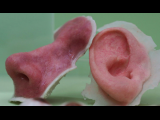
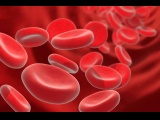
Регенеративная медицина — выращивание новых органов из стволовых клеток пациента с последующей заменой ими пришедших в негодность частей организма. Стимуляция процессов регенерации в организме. Использование выращенных органов и 3D печать. Уже сейчас можно выращивать некоторые органы из собственных клеток и сохранять стволовые клетки на будущее.
НАПРАВЛЕНИЯ РЕГЕНЕРАТИВНОЙ МЕДИЦИНЫ
▼ Материалы по теме
Регенеративная медицина — выращивание новых органов из стволовых клеток пациента с последующей заменой ими пришедших в негодность частей организма. В клиниках это научились успешно проделывать пока только с несколькими не очень сложными органами: трахеей, пищеводом, сосудами, но опыты на животных внушают оптимизм. Специалисты мечтают, что когда-нибудь необходимость в пересадке органов отпадет: мы научимся обновлять их с помощью собственных стволовых клеток прямо внутри тела.

Дорожную карту 2.0 можно посмотреть и скачать здесь: Версия 2.0 PDF.
Человек - это упорядоченная совокупность клеток, размноженных до конкретной степени. Сознание человека - это общение совокупности клеток некоторых типов. (Список клеток тела человека)
Организм челоека состоит из клеток суммой примерно 100 триллионов , или 1014. Все эти клетки возникли из одной клетки после оплодотворения.
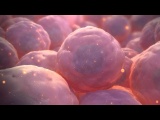
Сначала была одна стволовая клетка - Плюрипотентная (Зигота). После деления до 16 клеток, клетки становятся мультипотентными стволоыми. Они делилятся много раз, и достигнув определенного количества, становятся cтволовыи (эмбриональными). После следующего продолжительного цикла делений, стволовые клетки снова меняют тактику, становясь при делении своловыми (фетальными). Далее они, снова меняя тактику, становятся пуповинными, а затем уже постнатальными стволовыми клетками, то есть клетками взрослого человека. После 9-ти месячного формирования, человек рождается и продолжает формироваться. Стволовые клетки продолжают делиться по своей программе, и каждый орган немного увеличивается в размерах. Старые, поврежденные клетки отмирают, иногда становясь строительным материалом для других клеток. Но в течении жизни стволовых клеток становится все меньше, а старых клеток все больше. А еще в стволовых клетках накапливаются мутации, еще больше изменяя строение дочерних клеток. В итоге стволовые клетки одного или нескольких органов заканчиваются, либо ухудшается их качество.
Наибольший потенциал к регенерации характерен для эмбриональных стволовых клеток. Постнатальные и фетальные клеточные элементы также оказываются полезными, однако имеют ограниченный период существования, неширокий набор типов дочерних клеток и меньшие способности к регенерации.
Этапы развития стволовых клеток:
Плюрипотентная (Зигота (одна клетка)) -> мультипотентная (морула (с 2 до 16 клеток за 4-5 дней)) -> эмбриональная (бластоциста) -> фетальная -> пуповинная -> постнатальная
ВАМ НЕОБХОДИМО:
1. ДИАГНОСТИРОВАТЬ СВОИ СТВОЛОВЫЕ КЛЕТКИ
2. СОХРАНИТЬ СВОИ СТВОЛОВЫЕ КЛЕТКИ
а так же 4. НАЙТИ СПОСОБ ЕСТЕСТВЕННОГО ПОДДЕРЖАНИЯ ИХ НЕОБХОДИМОГО КОЛИЧЕСТВА В ОРГАНИЗМЕ
5. ИМЕТЬ ВОЗМОЖНОСТЬ КОРРЕКЦИИ ИХ ГЕНОВ
6. СЛЕДИТЬ ЗА МЕЖКЛЕТОЧНЫМ ПРОСТРАНСТВОМ И ВЗАИМОДЕЙСТВИЕМ КЛЕТОК
7. УНИЧТОЖАТЬ ИЗЛИШКИ СЕНЕСЦЕНТНЫХ КЛЕТОК
Приумножаем собственные плюрипотентные клетки.
Стволовые клетки, путем специальной обработки в центре биомедицинских технологий, получаем больших количествах.
3. ИМЕТЬ ВОЗМОЖНОСТЬ ВОСПОЛНЕНИЯ СТВОЛОВЫХ КЛЕТОК В ОРГАНИЗМЕ, ПУТЕМ РАЗМНОЖЕНИЯ "В ПРОБИРКЕ" СОБСТВЕННЫХ,
Клеточные технологии узаконили. Государственной Думой Российской Федерации принят Федеральный закон «О биомедицинских клеточных продуктах».
В середине 2016 года регенеративная медицина тала разрешенной и в России.
Также лечение стволовыми клетками можно получить и в рамках научного исследования. Для того, чтобы участвовать в таких исследованиях, нужно соблюсти некоторые правила:
- Есть программа исследований. которая определяет критерий включений и критерий исключений для пациента. Подписывается документ о добровольном участии в исследовании.
НОВОСТИ ВОСПОЛНЕНИЯ КЛЕТОК
Канадские ученые нашли способ выращивания стволовых клеток
В Японии впервые в мире имплантировали стволовые клетки
Стволовыми клетками начали спасать жизнь на Украине
В Китае расцвело нелегальное лечение стволовыми клеткам
Китай запретил лечение стволовыми клетками
НОВОСТИ РЕГЕНЕРАЦИИ
Ограниченное омоложение старых гемопоэтических стволовых клеток в молодой нише костного мозга
Гемопоэтические стволовые клетки (HSC) с возрастом обнаруживают функциональные изменения, такие как снижение регенеративной способности и миелоидно-зависимая дифференцировка. Ниша HSC, которая...
Читать далееРазведение плазмы улучшает когнитивные функции и снижает нейровоспаление у старых мышей
Наше недавнее исследование установило, что факторы молодой крови не являются причиной и не являются необходимостью для системного омоложения тканей млекопитающих...
Читать далееПора кончать со старой кровью - Джош Миттельдорф
2020 год обещает нам, что мы сможем сделать наши тела молодыми без явного восстановления молекулярных повреждений, но лишь просто изменив...
Читать далееОмоложение тканей трех зародышевых листков путем замены плазмы старой крови солевым раствором альбумина
Аннотация Гетерохронный обмен крови омолаживает старые ткани, и большинство исследований о том, как это работает, фокусируется на молодой плазме, ее фракциях...
Читать далееОбращение возраста: измерение эпигенетического возраста двух разных видов с помощью одних часов
Аннотация Известно, что молодая плазма крови оказывает благотворное влияние на различные органы у мышей. Однако не было известно, омолаживает ли молодая...
Читать далееТрансплантация ACE2-мезенхимальных стволовых клеток улучшает результат лечения у пациентов с пневмонией, вызванной COVID-19
Озвучить текст роботом:
Японцы получили разрешение скрестить эмбрион человека и животного
Ученые давно проводят эксперименты по выведению различных гибридных видов животных. Как правило, это относится к лабораторным животным, опыты над которыми...
Читать далееМыши смогли восстановить ампутированные пальцы при помощи двух белков
Возможно, в будущем люди смогут восстанавливать потерянные конечности — на это, во всяком случае, намекают медицинские эксперименты. Ученым уже известно...
Читать далееИзраильские учёные разработали универсальное лечение против рака
Небольшая группа израильских учёных считает, что они нашли первое универсальное лечение против рака. «Мы считаем, что через год мы предложим универсальное...
Читать далееУченые создают лазерный кожный регенератор из «Стартрека»
Технологии из научно-фантастической вселенной «Стартрек» продолжают проникать в нашу реальную жизнь. Мы уже читали о медицинском трикодере, слышали о разработках...
Читать далееКлеточная терапия без клеток: омоложение внеклеточными везикулами
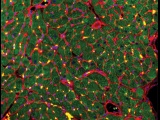
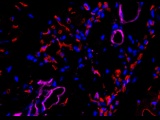
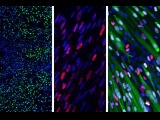
Восстановление сердечной мышцы после месяца терапии внеклеточными везикулами. Иммунные метки: агглютинин (красный), тропонин (зеленый) и DAPI (голубой) Исследователи Колумбийского университета, работающие...
Читать далееЛекарства от старения, и Где они обитают
Время напрямую людей не убивает, старение – это биологический процесс. Есть группа заболеваний, которые называют возраст-ассоциированными, или старческими. Основным фактором риска...
Читать далееИмплантация пигментного слоя сетчатки помогла сохранить зрение
Борьба с заболеваниями, которые в той или иной степени угрожают жизни человека – одно из самых приоритетных направлений современной медицины...
Читать далееУченым впервые удалось воссоздать легочную ткань
Лечение стволовыми клетками находит все большее применение в медицинской практике. Так, например, группа китайских ученых из Университета Тунцзи не так...
Читать далееПервый шаг к тканеинженерным надпочечникам
Исследователи лондонского университета королевы Марии, работающие под руководством доктора Леонардо Гуасти (Leonardo Guasti), использовали репрограммированные клетки для создания первого прототипа...
Читать далееВ Канаде появится фабрика по производству стволовых клеток
Правительство Канады недавно объявило о запуске проекта по созданию автоматизированного завода по производству стволовых клеток. Выращивание стволовых клеток может решить...
Читать далееПредставлен биопринтер, печатающий клетки поджелудочной железы для диабетиков
В настоящее время единственным спасением для пациентов, больных сахарным диабетом, являются регулярные инъекции инсулина. Однако давно ведутся исследования в сфере...
Читать далееМЕТАМОРФОЗ ЧЕЛОВЕКА
Бессмертие с помощью перерождения тела человека по достижению старения Давайте представим, каким в идеале должен быть человек, чтобы не умирать от...
Читать далееУченые разработали технологию, позволяющую массово выращивать клетки печени
Биологи из Японии и США продемонстрировали технологию, которая преодолевает основные препятствия в искусственном создании тканей печени человека, пригодных для терапевтической...
Читать далееПолностью функциональная искусственная сердечная мышца человека выращена в виде «заплаты» из перепрограммированных клеток
Исследователи из Университета Дьюка (Duke University) сообщили в журнале Nature Communications о том, что им удалось создать искусственную сердечную мышцу человека, размер которой покрывает...
Читать далееБезрубцовая регенерация
Удаление рубца, безрубцовое заживление после операции, перепрограммирование рубца в функциональную ткань. 1. Описание рубца. - скоро 2. Биомаркеры рубца. - скоро 3. Удаление рубца. - скоро 4...
Читать далееКлеточные трагедии, часть 4: Кем быть?
Внутренняя жизнь клетки насыщена событиями не меньше, чем человеческая. Она полна страстей и опасностей и так же неизбежно заканчивается смертью...
Читать далееКлеточные трагедии, часть 3: Шок!
Внутренняя жизнь клетки насыщена событиями не меньше, чем человеческая. Она полна страстей, опасностей и, как и всякая жизнь, рано или...
Читать далееКлеточные трагедии, часть 2: Жизнь в условиях стресса
Внутренняя жизнь клетки насыщена событиями не меньше, чем человеческая. Она полна страстей, опасностей и, как и всякая жизнь, рано или...
Читать далееКлеточные трагедии, часть 1: На грани самоубийства
Жизнь клетки насыщена событиями не меньше, чем человеческая. Она полна страстей, опасностей и, как и всякая жизнь, рано или поздно...
Читать далее3 НАЦИОНАЛЬНЫЙ КОНГРЕСС ПО РЕГЕНЕРАТИВНОЙ МЕДИЦИНЕ 2017
III Национальный Конгресс по регенеративной медицине проходил 15–18 ноября 2017 года в Москве, в Московском государственном университете имени М.в. Ломоносова. Представляем...
Читать далееВ ожидании чуда: Стволовые клетки: друг? враг? панацея?
Почти 110 лет с момента открытия. Более 26 000 научных статей только за последний год. Сотни клиник по всему миру обещают...
Читать далееОмоложение кроветворных стволовых клеток
На рисунке изображен дефект сосудистой стенки вследствие возрастных изменений: повышенное содержание активных форм кислорода (пурпурного цвета) в эндотелии сосудов костного...
Читать далееВ Японии впервые успешно пересадили ткани, напечатанные на 3D-принтере
Технология 3D-печати получает все большее распространение. И если каких-то 5 лет назад мы и подумать не могли о том, что...
Читать далееПути дифференцировки стволовых клеток
Дифференцировка стволовых клеток, то есть их превращение в тот или иной клеточный тип, — это сложный многоступенчатый процесс. По пути в конечное состояние клетка проходит...
Читать далееОт Долли к копии человека: неизбежная атака клонов
Валерий Спиридонов, первый кандидат на пересадку тела, рассказывает о том, как зародились современные технологии клонирования живых организмов, и рассуждает о последствиях их появления для человечества. Ключ жизни Начало...
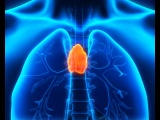
Читать далееПилотное исследование регенерации тимуса на людях
Авторы: Елена Милова, Стив Хилл Опубликовано наше со Стивом Хиллом интервью Грегори Фэя про его пилотное исследование регенерации тимуса на людях...
Читать далееТерапия стволовыми клетками эффективно и безопасно борется со старением
Американские и австралийские исследователи провели клинические испытания терапии стволовыми клетками для борьбы со старением. Метод оказался эффективным и безопасным для...
Читать далееКак вырастить стволовые клетки
Что такое стволовые клетки, как они влияют на жизнь человека и какие заболевания можно вылечить с их помощь? На эти и другие вопросы в интервью проекту...
Читать далееВпервые получена культура абсолютно универсальных стволовых клеток
Биологи впервые получили стволовые клетки, способные развиваться в клетки плаценты Сегодня у исследователей и медиков есть в распоряжении стволовые клетки...
Читать далееРоссияне получат доступ к выращенным в лабораториях тканям и органам
Клетки доросли до пациентов Выращенные в лабораториях ткани и органы будут доступны россиянам в следующем году. Больше 30 таких клеточных продуктов...
Читать далееСердечную недостаточность можно лечить стволовыми клетками пуповинной крови
Иногда медикаментозной терапии оказывается недостаточно, чтобы взять под контроль сердечную недостаточность. И тогда пациентам зачастую приходится вставать в очередь...
Читать далееУсы от собаки, иголки от ежа: как генетики создают абсолютно новых существ
Ученые-генетики ХХI века, благодаря прорывным открытиям в своей науке, все больше напоминают "лабораторных богов", которые владеют технологиями сборки "трехмерного генетического пазла" —...
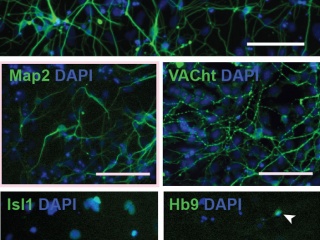
Читать далееУчёные превратили клетки человеческой кожи в двигательные нейроны
Двигательные нейроны человека трудно изучать, так как их невозможно отделить от живого пациента. Представленные на иллюстрации моторные нейроны получены...
Читать далее«Московский клуб покупателей» терапии от старения — план исследований
Начало здесь: Как победить старение - план действий Активисты борьбы со СПИДом в 1980-х По итогам моего предыдущего поста некоторые читатели упрекнули...
Читать далееКак победить старение - план действий
Старение — это генетическая патология, заложенная в каждого из нас. Это ВИЧ 2.0, неумолимая «возрастная инволюция человека». Я твёрдо верю...
Читать далееТеперь стволовыми клетками можно управлять при помощи магнита
Фрагмент колонии эмбриональных стволовых клеток человека (справа) и мышиные фибробласты Французские ученые ввели наночастицы железа в эмбриональные стволовые клетки мыши. Это...
Читать далееОрганы из пробирки: что уже умеют выращивать
Возможность вырастить человеческий орган в пробирке и пересадить его человеку, нуждающемуся в пересадке — мечта трансплантологов. Ученые по всему миру...
Читать далееВыращивание сосудов и регенерацияя конечностей перепрограммированными клетками кожи
Фибробласты Американские ученые из Университета Огайо создали новую технологию, с помощью которой можно перепрограммировать клетки кожи в другие виды клеток. Клеточную терапию...
Читать далееКонсервированные стволовые клетки остановят старение
Forever Labs, стартап из бизнес-инкубатора Y Combinator, консервирует стволовые клетки взрослых людей, чтобы помочь им продлить жизнь и молодость, пишет TechCrunch. Стволовые клетки могут стать...
Читать далееДжордж Чёрч – поворачивая время вспять
Предисловие Стива Хилла Многие из вас, наверное, уже знают профессора Джорджа Чёрча, ведь он является важным членом исследовательского сообщества, занимающимся лечением...
Читать далееВ Университете Огайо разработали чип, который может восстанавливать поврежденные ткани в считанные дни
Технологии в наше время развиваются настолько быстро, что разного рода новостям просто не успеваешь удивиться. То искусственный интеллект выигрывает в...
Читать далееНайден способ «перепрограммировать» клетки для лечения заболеваний
Не исключено, что с помощью нового метода можно будет восстанавливать не только мышечную, но и мозговую ткань. Ученые из Университета штата...
Читать далееКитайские ученые впервые успешно клонировали 13 свиней при помощи роботов
Как отмечают специалисты, использование робототехники позволило сделать все операции более точными, что сократило долю поврежденных клонированных клеток. Китайские специалисты впервые в...
Читать далееРоссийские ученые сделали очередной шаг на пути к регенеративной медицине
Новосибирские ученые на крысах изучили влияние малых некодирующих молекул рибонуклеиновой кислоты (микроРНК) на процесс превращения клеток, что позволит лучше понять этот сложный...
Читать далееНазвано средство против старческой немощи
Исследователи из медицинского центра при Рочестерском университете пришли к выводу, что с возрастной атрофией мускулов можно справиться, поддерживая существование мышечных...
Читать далееСибирские ученые исследуют способности стволовых клеток восстанавливать кровоток
Ангиогенез после введения стволовых клеток в тромбированную вену. Неокрашенные срезы в отраженном ультрафиолетовом свете с фильтром «Alexa 488». Сосуды и...
Читать далееКитай начинает первые в мире клинические испытания эмбриональных стволовых клеток
В двух новых клинических испытаниях в Китае начнут использовать эмбриональные стволовые клетки для лечения болезни Паркинсона и слепоты. Вместе с...
Читать далееБиологи научились заставлять клетки крови затягивать раны
Биологи из Канады открыли гормон, добавление которого в кровь "перепрограммирует" клетки иммунной системы и заставляет их приступить к ускоренной "починке" поврежденных слоев кожи и других...
Читать далееПечатающую стволовыми клетками биоручку протестировали на овцах
Специалисты австралийского Центра медицинских исследований Айкенхеда разработали особую «3D-биоручку», печатающую стволовыми клетками, ещё в прошлом году, но лишь сейчас получили...
Читать далееВ Санкт-Петербурге открылся центр клеточных технологий мирового уровня
В Институте цитологии РАН (Санкт-Петербург) открылся новейший Центр клеточных технологий (ЦКТ). Это первая в структуре РАН и ФАНО России исследовательская лаборатория, соответствующая...
Читать далееБиологи научились создавать кровь из стволовых клеток человека
Биологи из Бостона разработали методику превращения "перепрограммированных" стволовых клеток в заготовки клеток крови, что открывает дорогу для лечения болезней и создания "бесконечных" донорских запасов...
Читать далееУченые смогли из клеток кожи получить клетки мозга
Исследователям удалось перепрограммировать клетки кожи в стволовые клетки, а затем — в клетки мозга человека, которые необходимы для поддержания нейронных связей. Это достижение имеет...
Читать далееПуповинная кровь человека омолодила мозг мышей, заявляют ученые
Переливание человеческой пуповинной крови в кровеносную систему пожилой мыши омолодило ее мозг и улучшило память, заявляют ученые в статье, опубликованной в журнале Nature. "Нейрофизиологи постоянно...
Читать далееСосуды и кровь получили из клеток кожи коротким путем
Человеческие сосуды (фиолетовый цвет) и мышиные сосуды с имплантировавшимися человеческими клетками (красный цвет) в сердце мыши Американским ученым удалось получить клетки...
Читать далееГенетики научились получать из стволовых клеток любой тип тканей
Ученые Института биологических исследований Солка (США) при содействии Пекинского университета открыли химический коктейль, позволяющий выращивать из стволовых клеток как зародышевые, так...
Читать далееЗапущен портал с тысячами моделей стволовых клеток
Институт Аллена по изучению клеток запустил проект, посвященный стволовым клеткам. Одной из его составляющих стала коллекция трехмерных изображений стволовых клеток...
Читать далееМедики успешно применили стволовые клетки для лечения сердца
Ученые успешно применили "заплатки" из мускульных стволовых клеток для лечения людей, страдающих от сердечной недостаточности, говорится в статье, опубликованной в журнале JAHA. За последние два десятилетия...
Читать далееВпервые в мире пациенту пересадили донорские клетки сетчатки
Как сообщает издание The Japan Times, группе японских ученых из Института физико-химических исследований Рикен, что расположен в городе Вако, удалось...
Читать далееПроведена первая пересадка донорских индуцированных стволовых клеток
Впервые в истории медицины донорские индуцированные стволовые клетки были превращены в клетки сетчатки и пересажены пациенту. Житель Японии стал первым человеком...
Читать далееСтартап Organovo печатает на 3D-принтере клетки печени и почек
Компания разработала методику трехмерной печати живых тканей, с помощью которой можно создавать ткани печени и почек для последующей трансплантации в человеческий организм. Первые...
Читать далееТерапия стволовыми клетками помогла мужчинам справиться с эректильной дисфункцией
Лечение стволовыми клетками помогло мужчинам с эректильной дисфункцией Крупное достижение в исследованиях стволовых клеток дало возможность мужчинам с эректильной дисфункцией (возникшей...
Читать далееКак закон «О биомедицинских клеточных продуктах» отразится на российских инновациях
Закон, регулирующий использование клеточных технологий в России: начало новой отрасли, упрощение взаимодействия медицинского и бизнес-сообществ или осложнение совместной работы? Закон (ФЗ...
Читать далееТри женщины ослепли в результате лечения стволовыми клетками
Словосочетание «стволовые клетки» хорошо знакомо всем нашим читателям. Эти удивительные клетки, имеющиеся в теле многих живых организмов, способны превращаться в...
Читать далееОмоложение костномозговой ниши против старения
По мере старения человека стареют и его гемопоэтические стволовые клетки (ГСК), функция которых заключается в формировании всех типов клеток крови...
Читать далееРегенерацию сетчатки у рыб данио связали с ГАМК
Американские ученые показали, что гамма-аминомасляная кислота (ГАМК) регулирует процессы регенерации в сетчатке рыб данио-рерио. Результаты исследования опубликованы в журнале Stem...
Читать далееСтволовые клетки: руководство по эксплуатации
Насколько клеточные технологии и в частности стволовые клетки можно уже сейчас применять? Насколько это безопасно? Как не ошибиться в выборе...
Читать далееВпервые живой эмбрион вырастили из стволовых клеток
Бластоциста, выращенная in vitro, на четветые сутки (слева). Бластоциста на вторые сутки (справа). Красным цветом показаны эмбриональные стволовые клетки, синим...
Читать далееРассеянный склероз удалось «заморозить» на 5 лет
«Перезагрузка» иммунной системы, смогла, как минимум, на 5 лет остановить прогрессирование рассеянного склероза у 60-68% больных, прошедших процедуру трансплантации стволовых клеток. Об...
Читать далееБиологи продолжают исследовать процесс клеточного воскрешения
Несмотря на то, что современная наука бессильна против гибели клеток живого организма, некоторые исследователи с оптимизмом смотрят в будущее и...
Читать далееКости, хрящи и мышцы вырастили из одной стволовой клетки
хрящевая, костная и мышечная ткань, полученные из человеческих плюрипотентных стволовых клеток Биоинженерам из Калифорнийского университета удалось впервые получить из человеческих плюрипотентных...
Читать далееСредство для лечения рака может помочь перенёсшим инфаркт
Новый противоопухолевый препарат — средство пока находится в разработке — обеспечивает восстановление повреждённой сердечной мышцы. Это неожиданное открытие в будущем может привести к появлению лекарства...
Читать далееКФУ планирует вывести разработанные методики генной и клеточной терапии на всероссийский уровень
На территории Республиканской клинической больницы состоялся семинар, в котором приняли участие научные сотрудники ИФМиБ КФУ, врачи университетской клиники и РКБ. Поводом...
Читать далееУченые испытали методику омоложения со смертельным исходом
Исследователи испытали новую методику, позволяющую омолодить организм мышей. Правда, ее использование ведет к образованию опухолей, от которых грызуны умирают. Клетки зародыша...
Читать далееИскусственные клетки обманули бактерии, выдав себя за настоящие
Недавно исследователи из Италии справились со своего рода с микроскопической версией теста Тьюринга, создав искусственные клетки настолько реалистичными, что обыкновенные...
Читать далееСоздана химера человека и свиньи. Подробности
Немного расширенной информации по недавно созданой химере человека и свиньи Ученые впервые создали химеры человека и свиньи, что вызывает...
Читать далее3D-принтер на Arduino печатает функциональную человеческую кожу
По оценке ВОЗ, ежегодно около 11 млн пациентов в мире нуждаются в пересадке кожи после ожогов, а у 265 тыс. пострадавших повреждения...
Читать далееУченые обнаружили способ регенерации кожи без шрамов
Человеческий организм способен на поистине удивительные вещи. Однако, несмотря на миллионы лет эволюции и совершенствования своих способностей справляться с не...
Читать далееПочему люди не могут заново отращивать части тела. Видео
Современная наука позволяет выращивать человеческие органы и конечности. А насколько мы далеки от того, чтобы вырастить целый организм человека? Вы когда-нибудь...
Читать далееНамагниченные стволовые клетки против рака
Ученые лаборатории ТПУ разрабатывают способ управления клетками с помощью магнита Ученые лаборатории новых лекарственных форм Томского политехнического университета работают над созданием...
Читать далееРегенеративная медицина, базирующаяся на достижениях клеточных технологий
[row][column size="1/2"][/column] [column size="1/2"] Оглавление страницы: Экскурс в историюДоказательства обратимости старения. Перепрограммирование соматических клеток. Получение ИПСК.Клеточные технологии на основе ИПСК –...
Читать далееТехнологии регенеративной биологии и медицины в 21 веке
К сожалению, тело человека бренно, оно не приспособлено к тому, чтобы не изнашиваться, оно подвержено травмам, ранениям и ожогам. Органы...
Читать далееСозданы искусственные регенерирующие стволовые клетки
По сообщениям журнала Nature Communications, группа ученых из университета Северной Каролины совместно со своими коллегами из Китая разработали искусственные стволовые...
Читать далееПолучены данные доклинических исследований печени, созданной методом 3D-биопечати
Компания Organovo представила данные доклинических исследований искусственной человеческой печени, созданной методом органической 3D-печати. Результаты оглашены на конференции TERMIS-Americas, которая прошла...
Читать далееВыращены первые клетки биологического кардиостимулятора
Ученые из Макивеновского центра регенеративной медицине при университете Хита (США), под руководством постдока Стефани Протце (Stephanie Protze), впервые вырастили в...
Читать далееСоздание искусственных органов откладывается на год
Закон «О биомедицинских клеточных продуктах» не заработает с нового года из-за не принятых подзаконных актов С 1 января 2017 года вступает...
Читать далееУченые обратили вспять старение стволовых клеток
Микрофотография эмбриональных стволовых клеток человека Ученые из Школы медицины университета Джона Хопкинса впервые омолодили эмбриональные стволовые клетки (ЭСК) человека с помощью...
Читать далееКитайские исследователи успешно вживили искусственные вены 30 обезьянам
Исполнительный директор китайской биотехнологической компании Revotek Кан Юйцзянь сообщил журналистам о прорыве в области создания искусственных органов. Группа исследователей, работающих...
Читать далееЛожка честности в бочку патоки о регенеративной медицине. Интервью с Романом Деевым
Роман Деев, директор по науке ПАО «Институт Стволовых Клеток Человека». / Рисунок — Ася Ад. На недавно опубликованное у нас интервью с Еленой Губаревой...
Читать далееЛазер и стволовые клетки дают сердцу вторую жизнь
Кардиохирурги из Центра сердечно-сосудистой хирургии Бакулева начали проводить уникальные операции: с помощью лазера и стволовых клеток они спасают жизнь пациентам с тяжелой формой ишемической...
Читать далееСовременные методы лечения ССЗ — клеточная и генная терапии
Несмотря на широкий арсенал возможностей хирургии, сердечно-сосудистые заболевания (ССЗ) являются самой распространенной причиной смертности среди населения планеты. В настоящее время...
Читать далееЗапущен проект «Клеточный атлас»
Интегральный мембранный белок 2b (ITM2B). Изображение из базы Cell Atlas. В 2003 году был объявлен завершённым проект «Геном человека» (Human Genome...
Читать далееПробирка, принтер и ложные сенсации: как на самом деле выращивают органы
В век инноваций мы все чаще встречаем заголовки в стиле «Сенсация! Ученые вырастили сердце из стволовых клеток» или «Впервые в...
Читать далееУченые ищут способы регенерации тканей тела человека в генах кишечнодышащих
Все этапы регенерации кишечнодышащего червя Что было бы, если бы люди могли отращивать ампутированные конечности или полностью восстанавливать функции нервной...
Читать далееРоссийские ученые научились выращивать сетчатку глаза
Ученые ФМБА вырастили из клеток кожи человека сетчатку глаза, с помощью которой можно лечить слепоту В Федеральном научно-клиническом центре физико-химической медицины (ФНКЦ ФХМ) —подразделении Федерального медико-биологического...
Читать далееВ Австралии откроют центр по производству искусственных органов и тканей
О процессе 3D-печати биологических тканей и даже человеческих органов мы рассказывали вам на страницах нашего сайта неоднократно. Наука за последние...
Читать далееУченые завершили работу над 3D-атласом эмбриологии человека
Современная эмбриология шагнула достаточно далеко, но, несмотря на это, сам процесс развития и формирования человеческого эмбриона до сих пор скрывает...
Читать далееЗаработал банк стволовых клеток, выделенных из молочных зубов
В одной из шотландских лабораторий ученые начали вести сбор стволовых клеток из детских зубов. В дальнейшем клетки заморозят и они...
Читать далееПовреждения мозга у мышей удалось устранить за счет пересадки стволовых клеток
Мозг человека — это биологическое чудо с внушительными навыками. К сожалению, регенерации в их числе нет. За исключением одной маленькой...
Читать далееБелорусские ученые разработали способ выращивания кожи из клеток кожи пациента
Медики из Белоруси разработали инновационный метод выращивания человеческой кожи из клеток пациента. В данный момент выращенная таким образом кожа уже...
Читать далееКлетки крови сделали из клеток кожи
Ученые из Сингапура научились делать клетки крови из клеток кожи. Они провели эксперимент на мышах – созданные таким образом клетки...
Читать далееМышей омолодили человеческой кровью
Эксперименты по омоложению проводятся не первый год. В 2014 году Тони Висс-Корей (Tony Wyss-Coray) и его команда объявили о том, что...
Читать далееМини-легкие, выращенные в лаборатории, пересадили мышам
Американские исследователи из Университета Мичигана (University of Michigan) вырастили в лаборатории мини-легкие и пересадили их мышам. Трансплантация прошла успешно. Джейсон...
Читать далееВрачи растят ухо на руке пациента
Доктор Го Шучжун осматривает ухо, выращенное на руке пациента. Мужчина из Китая, последние годы живший без правого уха, скоро получит новое...
Читать далееВ области регенеративной медицины РФ идёт в ногу с Европой и Америкой
Сотрудники лаборатории фундаментальных исследований Международного научно-исследовательского клинико-образовательного центра регенеративной медицины. Регенеративная медицина находится в зачаточном состоянии. Но мечту вырастить орган «в пробирке» лелеют...
Читать далееСтволовые клетки – больше чем тренд
Антивозрастная терапия О стволовых клетках есть смысл говорить в двух контекстах: как о чем-то, что, постоянно находясь в нашем организме, поддерживает...
Читать далееИПСК: 10 лет спустя
Кора головного мозга человека культивируется в чашке Петри. Заболевания глаз лечатся с помощью клеток сетчатки, полученных из собственных клеток кожи...
Читать далееПересадка яичников омолодила пожилых мышей
Американские ученые обнаружили, что пересадка пожилым мышам яичников молодых животных обращает возрастные изменения метаболизма и иммунитета и приводит к продлению жизни...
Читать далееМожно ли обратить возраст стволовых клеток вспять?
Продолжительность жизни человека ограничена снижением количества стволовых клеток костного мозга с возрастом. Например, после 110 лет жизни примерно две трети белых кровяных...
Читать далееКомпания Organovo планирует запустить производство 3D-печатных живых тканей для трансплантации
Намерения инновационной компании подкрепляются успешными результатами клинических испытаний биопечатных образцов на лабораторных животных, продемонстрировавших живучесть, низкую вероятность отторжения и возможность...
Читать далееКомпания L’Oreal намеревается бороться с облысением с помощью аддитивных технологий
Содействие знаменитому производителю косметики оказывает французская компания Poietis, специализирующаяся на лазерной биопечати. Быстрых результатов партнеры не обещают, но в долгосрочной...
Читать далееУченые из России научились выращивать искусственные клетки
Сотрудники московского исследовательского центра клеточных технологий Института пластической хирургии и косметологии совместно со своими коллегами из НИИ хирургии детского возраста...
Читать далееЯпонцы научились трансплантировать донорские стволовые клетки без иммунодепрессантов
Японские биологи разработали технику трансплантации индуцированных плюрипотентных стволовых клеток (iPSC) от донора, не требующей применения иммунодепрессантов. Результаты работы представлены в...
Читать далееПациента с болезнью Паркинсона пробуют вылечить инъекциями стволовых клеток
Исследовательская группа из Королевской больницы Мельбурна (Royal Melbourne Hospital) приступила к испытаниям экспериментальной методики лечения болезни Паркинсона. Они ввели в головной...
Читать далееАнтиэйджинг – стволовые клетки и старение
1. Введение В широком смысле старение является нормальным прогрессирующим процессом, сопровождающимся усугублением предрасположенности к заболеваниям и смерти. Тот факт, что процесс...
Читать далее